タイFDA管轄製品 輸入販売の実務ポイント
- ASEAN・海外展開
- # 寄稿記事
最終更新日:
公開日:

前回は、タイFDAの認証取得プロセスについて説明しました。今回は、その中でも輸入製品登録時に必要な対応事項について、さらに詳しく解説します。また、実際にFDA管轄製品を輸入し、タイ国内で販売する前に把握しておきたい流通フローや留意点についてもご紹介します。
目次
輸入製品登録時の対応事項
FDAオンライン申請システムの開設後、輸入事業者の登録が完了したら、次に輸入製品の登録を行います。その際に求められる、他国とは異なるタイFDA特有の対応事項は以下の通りです。なお、登録に必要な書類は製品によって異なります。
1. 製品情報の開示
輸入製品登録時には、製品情報(成分表や製造工程など)の開示が必須です。特に、食品や美容・化粧品の場合、含有成分の100%開示が求められます。輸入製品が自社製品でない場合は、製造メーカーに書類や情報の提供を依頼する必要があり、情報開示の可否が重要な事前確認事項となります。
2. 官公庁や第三者機関発行の書類の提出
当該製品の製造国の官公庁が発行する公的証明書(自由販売証明書など)や、第三者機関が発行する書類(ISO認証取得証明書や試験成績書など)の提出が求められる場合があるため、各書類の取得方法や所要期間も事前に確認する必要があります。書類が英語版で発行されていない場合や、タイ語版の提出が必要な場合には、翻訳証明の取得が必要になることもあります。
3. 公証および領事認証
書類によっては、公証または領事認証が必要となります。各書類は発行国で取得する必要があり、日本で取得する場合は、公証人役場、法務局、または在日タイ大使館が申請先となります。日本以外の国で発行された書類については、その国での手続きが必要となり、取得方法が異なるため、時間を要することが多い点にも留意が必要です。
4. タイ語のラベル表示
製品登録時には、FDA管轄部署および製品区分に基づいて規定されたラベルの提出が必要となります。ラベル表示内容は製品の定義によって異なりますが、タイ語で作成し、ラベルを貼付するか、製品パッケージ(製品および梱包箱など)に印字して、消費者が製品販売時に認識できるよう義務付けられています。
輸入販売時の留意点
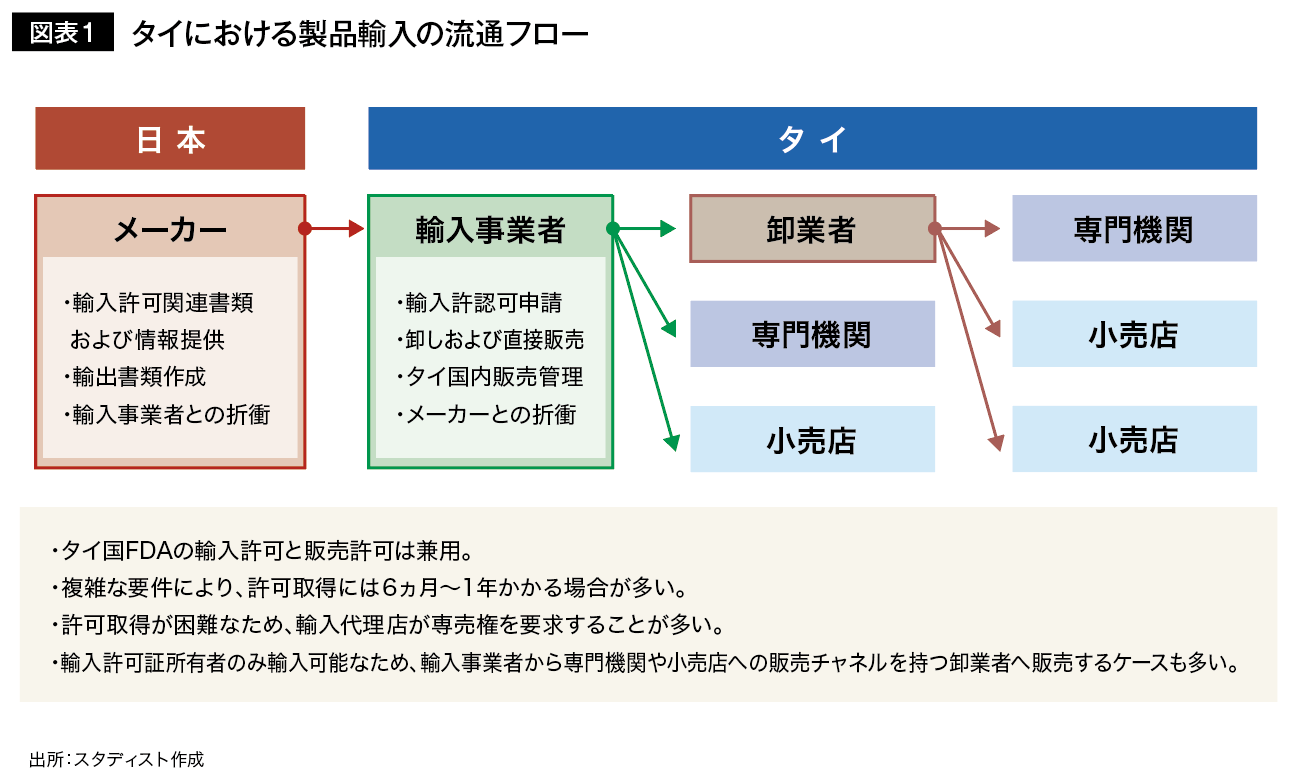
煩雑な登録手続きを経てFDAの認可を取得すると、タイへの製品輸入および国内販売が可能になります。製品輸入の流通フローは図表1のとおりです。ただし、FDA管轄製品は、原則として製品登録時の輸入事業者名義でのみ通関が可能であり、販売や広告に関する規制も遵守する必要があります。以下に、実際の輸入や販売時に注意すべき主なポイントをまとめます。
1. 複数の輸入事業者による製品登録
同じ製品を複数の輸入事業者で製品登録することも可能ですが、既に登録済みの製品名やパッケージの改定が求められる場合や、申請が不受理となる場合があります。
2. 輸入事業者登録の変更
何らかの理由で当該製品の輸入事業者登録を変更する場合、製品名やパッケージの改定が求められる場合や、申請が不受理となる場合があります。そのため、現行の輸入事業者による製品登録を先にキャンセルし、新たに申請することが推奨されます。
3. オンライン販売
タイ現地法人が未設立、または輸入代理店が決定していない場合、越境ECでの製品販売を検討することも多いかと思います。しかし、当該製品がFDAに未登録の場合、通関は当然不可能です。税関で差し止められ、販売先への配送が完了しない事例も多発しています。タイFDA管轄製品の越境EC展開は不可であることをご認識ください。また、タイ国内でオンライン販売を行う際には、タイ商務局でEC事業の登録が必要となります。
4. 広告
FDA管轄製品の広告は、事前に広告内容の審査および承認を受ける必要があります。承認されていない広告物の掲載や流布はもちろん、オンライン広告もすべて対象となります。
タイでのFDA管轄製品の輸入販売においては、万全の事前準備を整えて臨んでも、申請プロセス中に追加書類の提出などの指摘を受けることが多いのが実情です。そのため、事前準備は最低限にとどめ、申請開始後に指摘事項に随時対応していく柔軟なアプローチが推奨されます。